-
טופס 1: בקשה לביצוע מחקר
-
טופס 2: טופס הסכמה מדעת לבגיר
-
טופס 3: הסכמה מדעת להורי קטין
-
טופס 4: התחייבות יזם המחקר
-
טופס 5: הצהרת היזם לסיווג המחקר
-
טופס 6: אישור ועדת הלסינקי לביצוע מחקר (טופס 6א: אישור הארכה)
-
טופס 7: אישור מנהל המוסד הרפואי לביצוע המחקר (טופס 7א: אישור הארכה)
-
טופס 8: אישור משרד הבריאות לביצוע מחקר
-
טופס 9: הצהרת היזם ואישור קבלת מסמכי המחקר על ידי רכז הוועדה
-
טופס 10: בקשה לפרסום המחקר בקהילה
-
טופס 11: מכתב לרופא המטפל
-
טופס 12: בקשה לשינויים במחקר
-
טופס 13: הודעה על אירוע חריג
-
טופס 14: הודעה על פטירת משתתף במחקר
-
טופס 15: דוח תקופתי למשרד הבריאות
-
טופס 16: אישור תת ועדת הלסינקי לביצוע מחקר שאלונים/רטרוספקטיבי (טופס 16א: אישור הארכה)
-
טופס 17: אישור מנהל המוסד הרפואי לביצוע מחקר שאלונים/רטרוספקטיבי (טופס 17א: אישור הארכה)
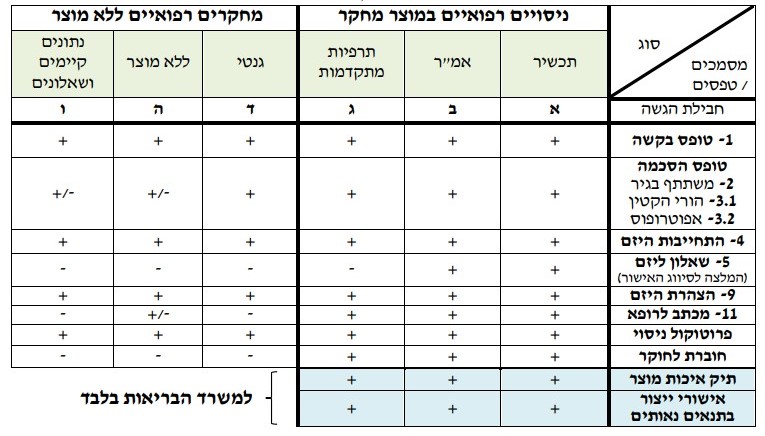
לכל סוג ניסוי רפואי קיימת חבילת הגשה נפרדת, כמתואר בטבלה מספר 1 להלן:
א' - ניסוי בתכשיר
ב' - ניסוי באמ"ר
ג' - ניסוי בתרפיות מתקדמות
ד' - ניסוי גנטי
ה' - ניסוי ללא מוצר מחקר
ו' - מחקר בנתונים קיימים ושאלונים
טבלה מספר 1: מסמכי ההגשה הנדרשים עבור בקשה לניסוי רפואי בבני אדם